פריצת דרך בחקר האוטיזם: נחשפו מנגנונים מוחיים המעורבים באוטיזם שמקורו גנטי
חוקרים מאוניברסיטת תל אביב הצליחו ליישם טיפול גנטי שהצליח לשפר את תפקוד התאים הפגועים במוטציה בגן SHANK3, שמובילה למקרים רבים של אוטיזם בעולם
חוקרים מאוניברסיטת תל אביב הצליחו ליישם טיפול גנטי שהצליח לשפר את תפקוד התאים הפגועים במוטציה בגן SHANK3, שמובילה למקרים רבים של אוטיזם בעולם
מחקר חדש ופורץ דרך של צוות מחקר מבית הספר למדעי הפסיכולוגיה מרחיב את ההבנה לגבי הגורמים לאוטיזם שמקורו גנטי, ובפרט מוטציות בגן SHANK3, שאחראיות לכמעט מיליון מקרים של אוטיזם ברחבי העולם. לאור התגליות, יישם צוות המחקר טיפול גנטי שהצליח לשפר את תפקוד התאים שנפגעו מהמוטציה. לדברי החוקרים, בכך הונחה תשתית לפיתוח עתידי של טיפולים יעילים לאוטיזם שמקורו גנטי.
מה מפריע להעברת מסרים בין אזורי המוח?
המחקר הובל על ידי מעבדתו של פרופ' בועז ברק והדוקטורנטית ענבר פישר מבית הספר סגול למדעי המוח ומבית הספר למדעי הפסיכולוגיה בפקולטה למדעי החברה ע"ש גרשון גורדון, בשיתוף עם מעבדותיהם של פרופ' בן מעוז מהמחלקה להנדסה ביו-רפואית בפקולטה להנדסה ע"ש איבי ואלדר פליישמן, ופרופ' שני שטרן מהמחלקה לנוירוביולוגיה באוניברסיטת חיפה. המאמר פורסם בכתב העת היוקרתי Science Advances.
"אוטיזם הוא הפרעה נוירו-התפתחותית שכיחה, הנגרמת ממגוון גורמים, בהם מוטציות גנטיות", מסביר פרופ' ברק. במעבדתו נחקרת מוטציה בגן SHANK3, האחראית לכ-1% ממקרי האוטיזם בעולם. "חלבון שמקודד על ידי SHANK3 ממלא תפקיד קריטי בעיגון קולטנים החיוניים לתקשורת בין תאי עצב, ולכן פגיעה בו משבשת את פעילות המוח. המחקר הנוכחי שלנו מתמקד במנגנונים חדשים ולא מוכרים שבהם המוטציה משפיעה על התפתחות המוח, וגורמת לליקויים הקשורים לאוטיזם".
צוות המחקר התמקד בשני מרכיבים במוח שטרם נחקרו לעומק בהקשר זה: תאי תמך שנקראים אוליגודנדרוציטים, ורקמת המיאלין שמיוצרת על ידם. רקמת המיאלין הינה רקמה שומנית העוטפת את שלוחות תאי העצב (אקסונים), ומשמשת כחומר מבודד, בדומה לשכבת הבידוד העוטפת כל כבל חשמלי שאנחנו מכירים. כאשר המיאלין אינו תקין, האותות החשמליים העוברים בשלוחות עלולים לזלוג החוצה, וכך משתבשת העברת המסרים בין אזורי המוח, והתפקוד המוחי נפגע. הצוות נעזר בהנדסה גנטית כדי ליצור מודל לאוטיזם בעכברים, על ידי גרימת מוטציה בגן SHANK3, שזהה בדיוק למוטציה הקיימת אצל בני אדם עם סוג זה של אוטיזם.
"באמצעות המודל מצאנו שהמוטציה בגן גורמת לפגיעה כפולה בהתפתחות ובתפקוד התקין של המוח: ראשית, גילינו שכמו בתאי העצב, גם באוליגודנדרוציטים, החלבון SHANK3 הינו קריטי לעיגון ולתפקוד התקין של קולטנים הקולטים אותות כימיים (נוירוטרנסמיטורים ואחרים) מתאים שכנים. המשמעות היא שהחלבון הפגום המאפיין אוטיזם משבש את העברת המסרים לתאי התמך החיוניים הללו. שנית, בעקבות הפגיעה בתפקוד ובהתפתחות של האוליגודנדרוציטים משתבש גם ייצור המיאלין על ידם. המיאלין הפגום אינו מבודד כראוי את שלוחות תאי העצב, וכך פוגע ביעילות הולכת האותות החשמליים בין תאי המוח ובסנכרון הפעילות החשמלית בין אזורי המוח השונים. במודל שלנו מצאנו פגיעה במיאלין באזורים רבים במוח, וראינו שהתנהגות העכברים נפגעה כתוצאה מכך".

פרופ' בועז ברק והדוקטורנטית ענבר פישר
לתקן את מה שמקולקל
בהמשך ביקשו החוקרים לבחון שיטה אפשרית לתיקון השיבוש שנגרם על ידי המוטציה, בתקווה שניתן יהיה בעתיד להשתמש בגישה זו גם בבני אדם. "הפקנו אוליגודנדרוציטים ממוח של עכבר עם מוטציה בגן SHANK3, ובאמצעות טיפול גנטי החדרנו לתוך התאים מקטע DNA המכיל את הרצף התקין של הגן SHANK3 האנושי. המטרה הייתה לאפשר לגן התקין לקודד חלבון תקין, אשר יוכל לבצע את התפקיד החיוני בתא, במקום החלבון הפגום. ואכן, לשמחתנו, תאים עם מוטציה שטופלו בטיפול הגנטי ביטאו חלבון SHANK3 תקין, שאיפשר בנייה של מערך חלבונים תקין לעיגון הקולטנים הדרושים לקליטת האותות החשמליים. במילים אחרות: הטיפול הגנטי שפיתחנו תיקן את אתרי התקשורת באוליגודנדרוציטים, אשר חיוניים להתפתחות ולתפקוד תקין של תאים אלה לשם ייצור המיאלין במוח", מסבירה ענבר פישר.
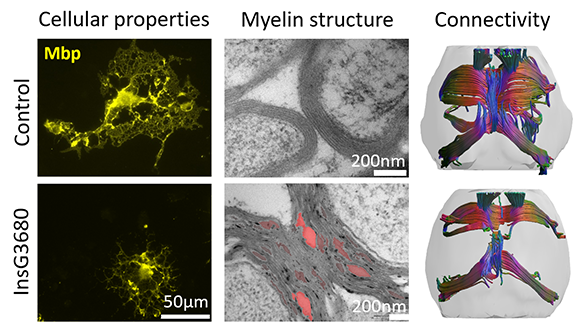
בטור השמאלי: אוליגודנדרוציטים, גדולים ומפותחים ומיצרים מיאלין באופן תקין בחיה בריאה, ואצל חיות המודל לא. בטור האמצעי: צילום במיקרוסקופ אלקטרונים של המיקרוסטרוקטורה של המיאלין. בטור מימין: הקישוריות המוחית. ככל שיש יותר סיבים (אקסונים) ועליהם יותר מיאלין, נראה יותר מסילות צבעוניות שמקשרות בין איזורי מוח שונים
כדי לתקף את הממצאים מעכברי המודל הפיק צוות המחקר תאי גזע מתאי עור של נערה עם אוטיזם כתוצאה ממוטציה בגן SHANK3 (זהה לזו שבעכברים). מתאי גזע אלה יוצרו אוליגודנדרוציטים אנושיים שהמטען הגנטי שלהם זהה בדיוק לזה של הנערה. באוליגודנדרוציטים הללו נמצאו בעיות דומות לאלה שהתגלו במקביליהם העכבריים.
פרופ' ברק מסכם כי המחקר חשף שני מנגנונים חדשים באוטיזם גנטי: פגיעה בתאי התמך מסוג אוליגודנדרוציטים, שמובילה לפגיעה במיאלין. "ממצא זה חשוב להבנת אוטיזם, כיוון שמדגיש את תפקידו של מיאלין פגום במחלה ואת תפקודו של חלבון SHANK3 בשמירה על מצע לקליטת מסרים. בהיבט הרפואי, המחקר מצביע על הצלחת טיפול גנטי לשיפור תפקוד האוליגודנדרוציטים בעכברים, מה שמאפשר תקווה לפיתוח טיפולים גנטיים לבני אדם, אשר יובילו בין היתר לתיקון תהליך ייצור המיאלין במוח. בנוסף, עצם ההבנה שלפגיעה במיאלין יש חשיבות באוטיזם (עם או בלי קשר לגן SHANK3) פותחת כיוונים חדשים להבנת המנגנונים המוחיים המעורבים באוטיזם, כמובן בשאיפה לפיתוח טיפולים עתידיים".







